比熱
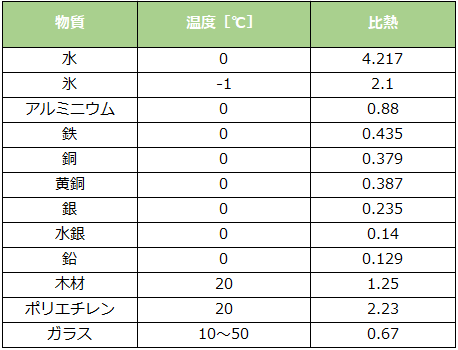
比熱(ひねつ、specific heat capacity)とは熱の伝わりやすさで、温度を1℃(K)あげるのに必要な熱量のことをいい、体積が一定のものが定容比熱、圧力が一定のものが定圧比熱という。現実では、体積・圧力ともに異なるため、理想気体を想定して考察されている。また、定圧比熱と定容比熱との比を比熱比という。
比熱の定義と物理的意味
比熱は、物質の質量をm、加えた熱量をQ、それによる温度変化をΔTとしたとき、式 c = Q / (mΔT) によって定義される。この式における c が比熱であり、物質がどれだけのエネルギーを内部エネルギーとして蓄えられるかを示している。ミクロな視点では、物質を構成する原子や分子の運動(振動、回転、並進)に費やされるエネルギーの総和が、マクロな温度上昇として現れる。エネルギーの保持能力が高い物質ほど、外部から熱を与えても温度が上がりにくいという特性を持つ。
熱容量と比熱の違い
比熱としばしば混同される概念に「熱容量」がある。熱容量は物質全体(例えば製品一個や装置一台)の温度を1K上げるのに必要な熱量であり、物質の質量に依存する。これに対し、比熱は単位質量あたりの値であるため、物質の種類が同じであれば質量に関わらず一定の値をとる。したがって、熱容量 C は、物質の質量 m と比熱 c の積(C = mc)として算出される。設計現場では、特定の部品が保持する全熱量を知るために熱容量が計算され、その基礎データとして材料ごとの比熱が参照される。
定容比熱
定容比熱とは、容量が一定の条件で、単位質量の物質の温度をあげるのに必要となる熱量のことをいう。
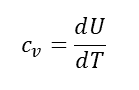
定圧比熱
定容比熱とは、定圧の一定の条件で、単位質量の物質の温度をあげるのに必要となる熱量のことをいう。
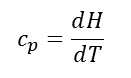
マイヤーの関係
マイヤーの関係とは、定圧比熱と定容比熱の差は気体定数になるという関係で、このことは、定圧比熱は常に定容比熱よりも大きいことを示している。
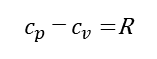
比熱比
比熱比とは、定圧比熱と定容比熱との比である。理想気体の比熱比は単原子気体で5/3、2原子気体では7/5、多原子気体では4/3となり、原子数が少ないほど大きくなる。
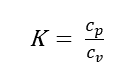
主な気体の気体定数、比熱、比熱比K
| 気体 | 気体定数R [J /(kg・K)] |
定圧比熱 cp [J /(kg・K)] |
定容比熱 cv [J /(kg・K)] |
比熱比 K |
|---|---|---|---|---|
| ヘリウム He | 2076.900 | 5.197 | 3.120 | 1.666 |
| 水素 H2 | 4124.000 | 14.320 | 10.190 | 1.405 |
| 窒素 N2 | 296.790 | 1.040 | 0.744 | 1.399 |
| 酸素 O | 259.820 | 0.915 | 0.655 | 1.397 |
| 空気 | 286.990 | 1.006 | 0.719 | 1.399 |
| 一酸化炭素 CO | 296.820 | 1.043 | 0.746 | 1.398 |
| 一酸化窒素 NO | 277.080 | 0.995 | 0.718 | 1.386 |
| 二酸化炭素 CO2 | 188.910 | 0.850 | 0.661 | 1.286 |
| アンモニア NH3 | 488.200 | 2.156 | 1.668 | 1.293 |
| メタン CH | 518.230 | 2.232 | 1.714 | 1.302 |
先端材料と比熱設計
次世代の産業技術においても、比熱の制御は鍵を握っている。例えば、電気自動車(EV)のバッテリーマネジメントシステムでは、セルの比熱を考慮した精密な温度制御が寿命と安全性に直結する。また、相変化材料(PCM)を利用した蓄熱装置では、特定の温度域で実質的に無限大に近い「見かけの比熱」を利用することで、高効率なエネルギー貯蔵を実現している。極低温工学や宇宙開発など、極限環境下での熱設計においても、物性としての比熱の正確な把握がプロジェクトの成否を分ける。

コメント(β版)