カルノーサイクル Carnot cycle
カルノーサイクルとは、フランスのカルノー(Nicolas Leonard Sadi Carnot)によって考案された、高温熱源から熱エネルギーを得て、その一部から仕事を行い、残りの熱を低温熱源に戻す、という熱機関のサイクルである。ただし、等温変化で受熱と排熱をするため、カルノーサイクルで作動する内燃機関は存在しなせず、理論最大熱効率を考察するための理想モデルである。
理論を支える歴史的背景とカルノーの洞察
ニコラ・レオナール・サディ・カルノーがカルノーサイクルを構想した当時、熱が「カルリック(熱素)」と呼ばれる物質であると考えられていた時代であった。カルノーはこの誤った熱素説を前提にしながらも、熱機関が仕事を発生させる条件が「高い温度から低い温度への熱の移動」にあることを鋭く見抜いた。これは水車が高い所から低い所へ流れる水を利用して動力を得るメタファーに近い着想であった。彼は特定の作動流体(水蒸気や空気など)に依存しない普遍的な法則を追い求め、摩擦や無駄な熱漏れが一切ない「可逆性」を備えた理想的なサイクルを定義した。この抽象化こそが、現代の機械工学や化学工学における熱力学的分析の基礎を築いたのである。
状態変化を構成する4つの過程
カルノーサイクルは、シリンダー内の理想的なガスなどの作動流体が以下の4つの過程を順に経ることで1サイクルを完結させる。
- 等温膨張(Isothermal Expansion):高温の熱源(温度 TH)から熱 QH をゆっくりと受け取り、作動流体の温度を高温のまま一定に保ちながら膨張する過程である。受け取った熱エネルギーはすべて外部への仕事に変換され、内部エネルギーは変化しない。
- 断熱膨張(Adiabatic Expansion):外部との熱のやり取りを完全に断ち切った状態で、作動流体がさらに膨張する過程である。膨張によって自らの内部エネルギーを消費して外部へ仕事を行い、その結果、作動流体の温度は低温熱源と同じ温度 TC にまで低下する。
- 等温圧縮(Isothermal Compression):低温の熱源に対して熱 QC を放出しながら、温度 TC を一定に保ちつつ外部から仕事をされて作動流体が圧縮される過程である。系を元の状態に戻すために必要な最小限の排熱が行われる。
- 断熱圧縮(Adiabatic Compression):再び外部との熱のやり取りを完全に断ち、外部から仕事をされて作動流体が圧縮される過程である。外部からの仕事によって内部エネルギーが上昇し、作動流体の温度は元の高温熱源の温度 TH に戻り、サイクルが完了する。
カルノーサイクルのモデル
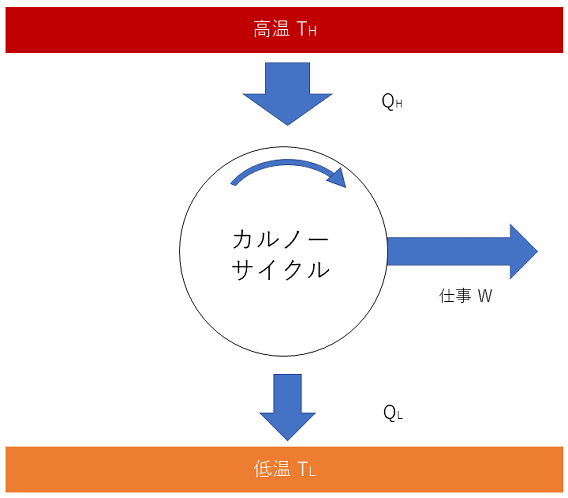
カルノーサイクルのモデルとは、温度THの高温熱源から熱量QHを取り入れて、その一部を外部への仕事Wに変換してから、残りの熱量QLを温度TLの低温熱源へ捨てる、という動作を繰り返していくサイクルである。
P-V線図
P-V線図とは、物体の圧力Pと体積Vとを直交座標の両軸にとって状態変化を表した線図である。カルノーサイクルは2つの等温変化(等温膨張、等温圧縮)と2つの断熱変化(断熱圧縮、断熱膨張)の変化からなるもので、準静的過程と仮定した可逆サイクルである。
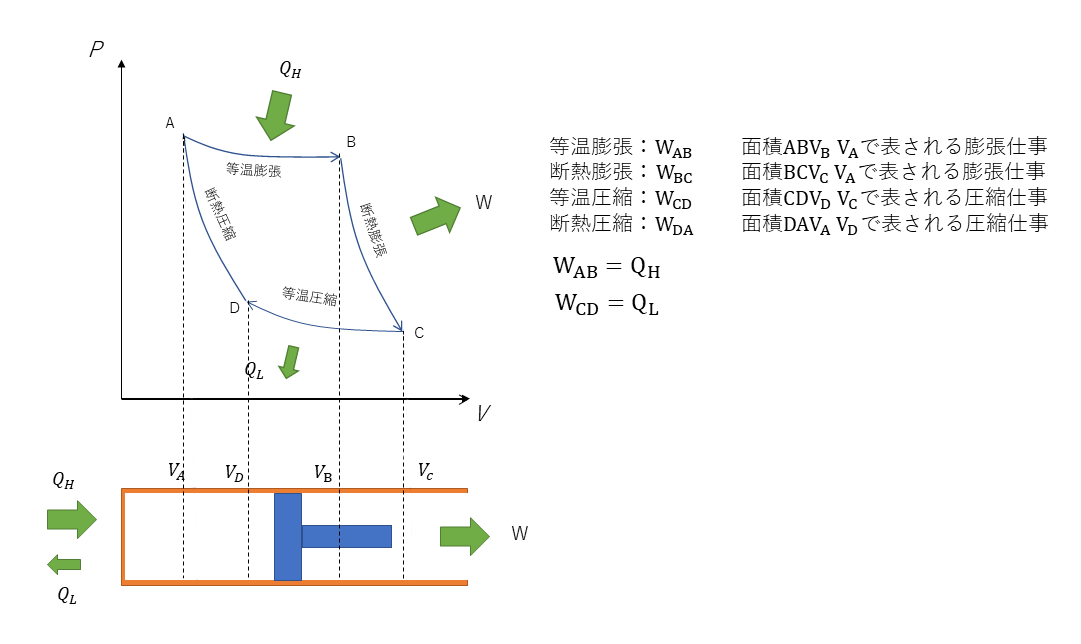
A→Bの過程:等温膨張
A→Bの過程とは、等温膨張の過程である。高温における等温給熱過程であり、シリンダ内の気体は、外部からの熱を吸収することによって、状態AからBに膨張していく。内部の温度は、温度THの高温熱源から熱量QHを取り入れて状態AからBに変化するので、準静的過程であるためには、高温熱源THと同じ温度で変わらず等温膨張となる。
B→Cの過程:断熱膨張
B→Cの過程とは、断熱膨張の過程である。 高温熱源からの熱量QHが遮断されて、状態BからCに膨張します。熱の出入りがなく膨張するために温度が下がり、低温熱源のTLに等しくなるまで膨張する。断熱変化で外に対して仕事Wをしているために、内部エネルギーは減少して温度はTHからTLに下がる。この過程は、断熱冷却の過程で断熱膨張となる。
C→Dの過程:等温圧縮
C→Dの過程とは、等温圧縮の過程である。内部の気体が低温熱源のTLと同じ温度になり、低温熱源に触れた状態で体積を減少させる過程となる。外部から仕事を得て、状態CからDに圧縮される間に熱が出るが、その熱量QLは温度TLの低温熱源へ捨てられる。この過程は、元の状態に戻すために必要な部分で、低温における等温放熱の過程で等温圧縮となる。
D→Aの過程:断熱圧縮
D→Aの過程とは、断熱圧縮の過程である。低温熱源から切り離されて、状態Dから最初のAに圧縮されて戻る。外部からの仕事を得て圧縮されるが、その間に熱が外に出ないため、内部の気体は高温熱源の温度THまで上昇する。この過程で元の状態に戻るが、断熱における昇温の過程で断熱圧縮となる。
T-S線図
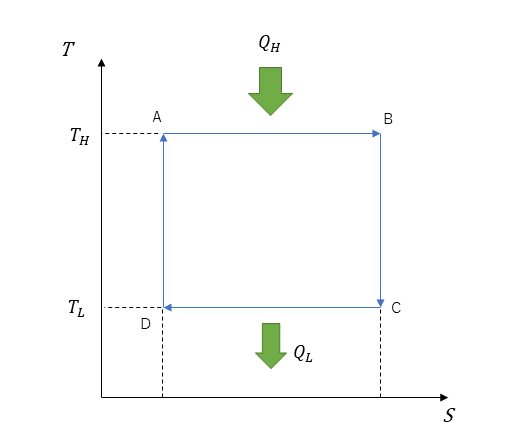
サイクル仕事
サイクル仕事は次式の通りになる。

カルノーサイクルの受熱量と排熱量の比
カルノーサイクルの受熱量と排熱量の比はQH/QL=TH/TLと表される。

カルノーサイクルのサイクル効率
カルノーサイクルのサイクル効率は下記の次式で表される。ここにおける熱効率とは、カルノーサイクルが高温熱源から受け取った熱量のうちの仕事に変換できた量を示す指標となる。 供給された熱量QHのうちで、外部に対して成す正味の仕事をWとして低温熱源へ捨てられる熱量をQLと考える。 A→B→C→D→Aのサイクルのなかで、この間に外部に行った仕事はW=QH-QLとなる。 なお、外燃機関であるスターリングエンジンの理論効率はカルノーサイクルと同じになる。(参考:スターリングサイクル)

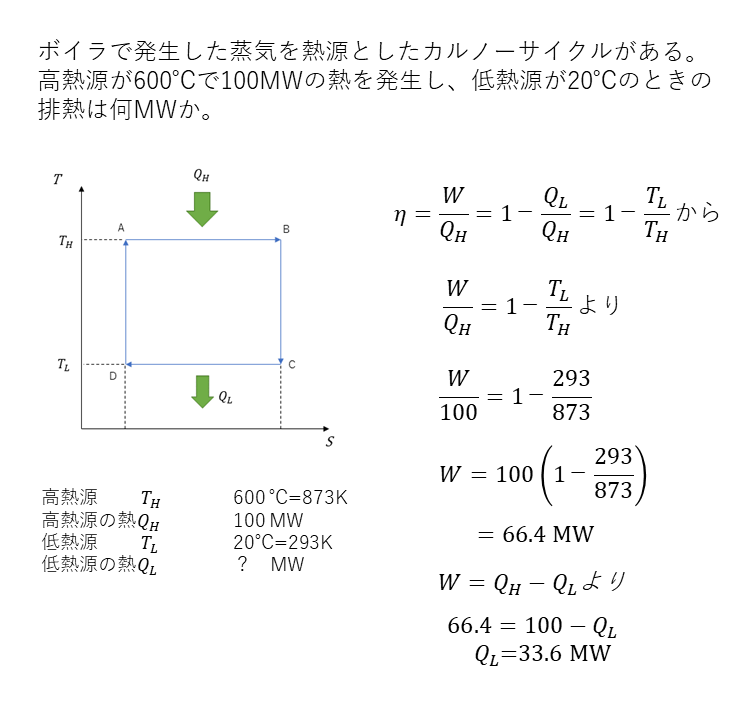
カルノーサイクルの計算例1
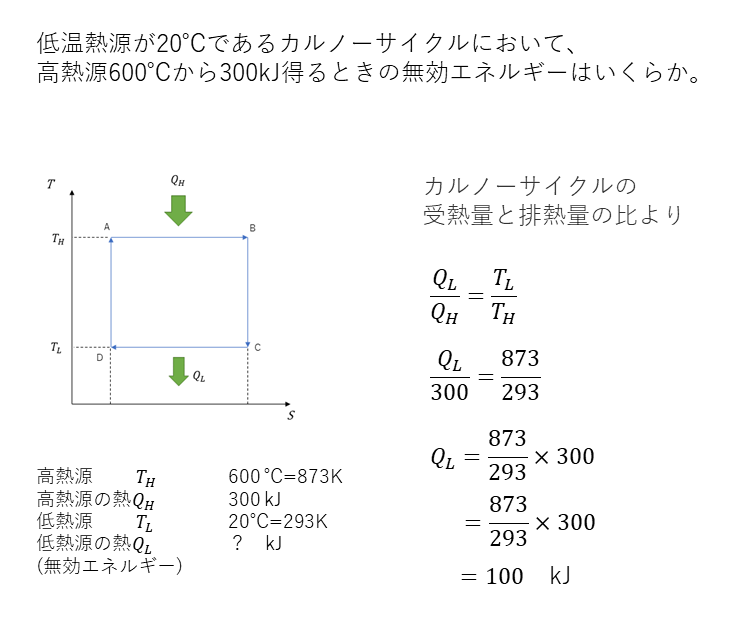
カルノーサイクルの計算例2
逆カルノーサイクル
逆カルノーサイクルとはカルノーサイクルの仕組みを逆にしたサイクルである。冷凍機やヒートポンプとして利用される。

コメント(β版)