熱量 heat quantity
熱量とは、物体が高温から低温に移動するときの熱エネルギーを量として考えたものである。SI単位ではジュール[J]を用いる。あるいは標準気圧のもとで1gの純粋な水を1°C高めるのに必要な熱量としてカロリー[cal]が使われる。(1cal=4.186J)下記に示される通り、熱量は質量に比熱と温度変化の積で求めることができる。また仕事と同じものとして扱うことができるため、熱量=仕事の方程式が成り立つ。
熱量の単位
熱量の単位は、工学的には標準気圧のもとで1gの純粋な水を1°C高めるのに必要な熱量を1calと定義される。通常は、SI単位系としてジュール[J]を用いる。1cal=4.186Jの換算式を用いる。(熱の仕事当量)
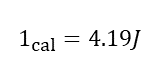
熱量
熱量は質量に比熱と温度変化の績で求められる。比熱とは物質に対しての温度変化のしやすさで、通常、比熱が低い物質ほど、熱しやすく冷めやすい性質といえる。

比熱
比熱は、物体の温度や圧力などの条件によって異なる定数で、温度の変化のしやすさ/しにくさを示す指標である。単位質量の物質の温度を1Kあげるために必要な熱量と定義される。単位としては、[kJ/(kg・K)] あるいは[kJ/(kg・°C)] を用いる。圧力を一定に保つ場合の比熱を定圧比熱Cp、体積を一定に保つ場合の比熱を定容比熱Cvという。一般に定圧比熱が定容比熱より大きくなるが、液体や固体では温度上昇による体積変化が小さいことから、これらの差は無視できるほど小さくなるため、通常は、比熱Cが用いられる。
| 比熱 [J/(g⋅K)] | |
|---|---|
| 水 | 4.2 |
| 氷 | 2.1 |
| なたね油 | 2 |
| アルミニウム | 0.88 |
| ステンレス | 0.46 |
| 鉄 | 0.44 |
| 銅 | 0.38 |
| 黄銅 | 0.387 |
| 鉛 | 0.13 |
| 銀 | 0.235 |
| 水銀 | 0.14 |
| ポリエチレン | 2.23 |
| ガラス | 0.67 |
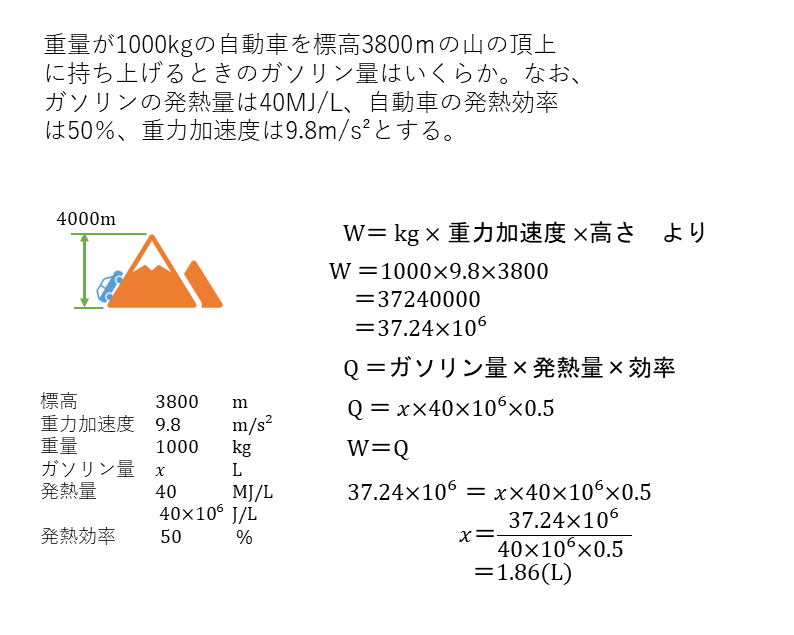
熱量の計算例1

熱量の計算例2
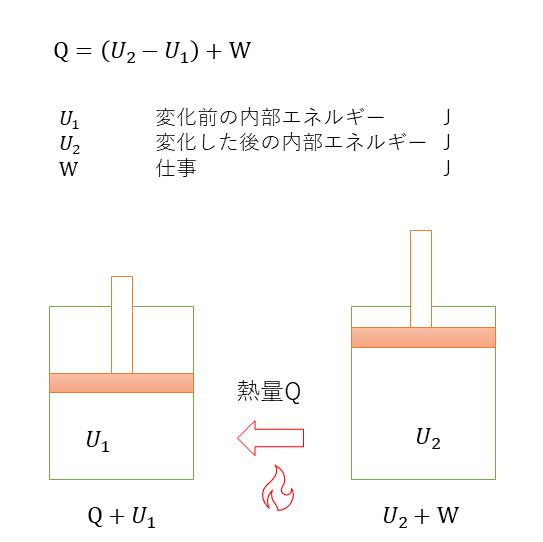
内部エネルギー
潜熱
潜熱とは、物質に熱を出入りさせて、その温度、圧力、化学組成 が一定のままで相変化をさせた場合に出入りする熱量である。単位は[J/kg]が使われる。物体の相変化、例えば氷が溶けて水になるような現象は、温度一定のもとで起こるが、熱エネルギーの移動に伴って温度変化が見えないことから名づけられた。

コメント(β版)