金属
金属(metal)とは、金属元素によって金属結合によってできた物質である。陽イオンが自由電子を媒介として強固な結合をしている。延性、展性に優れており、塑性変形が大きく機械加工を可能とする。電気や熱を伝えやすく、また、金属独特の光沢をもつのが特徴である。展性、塑性(延性)に富み、機械加工に優れているため、機械として主に使われる。また、電気および熱の良導体であり、金属光沢という特有の光沢を持つ。金属は個相(個体)、液相(液体)、気相(気体)の形態をもつ。

金属と歴史
金属の発展は人類史の発展とともにその歴史を歩んできた。もともと人類は石器を使い、次に青銅を扱うようになり、次第に金属を使うようになるが、金属の製造は生産革命を促した。人類の死亡率の低下や金属器の使い方は、社会を安定化することに成功した。特に18世紀の産業革命は、人々の生活を大きく変化させた。

金属特性
金属の一般的に下記の特性をもち、機械材料として広く利用されている。
- 常温で固体
- 硬度が高い
- 通電性がある
- 伝熱性がある
- 塑性変形が大きく加工性に優れている
- 表面に光沢をもつ
合金
金属は純度100%の純金属で使用されることは少なく、求める材料性質を得るため、金属に他の元素を混合・溶融して複合材料として利用することがある。この代表的なものが合金と呼ばれ、身近な金属の多くは合金で構成されている。一般に混合・溶解が進むと、その過程で結晶格子がひずみ、材料の強度が上がるためである。 (個溶強化)
結晶
金属は結晶粒と呼ばれる小さい結晶の粒の集まりで構成されている。結晶粒の多くが集まって結晶または結晶体をなす。結晶体は原子や分子がある規則的な配列に集合した固体であり、その結晶構造は、面心立方格子、体心立方格子、稠密六方格子の三種類に分かれる。
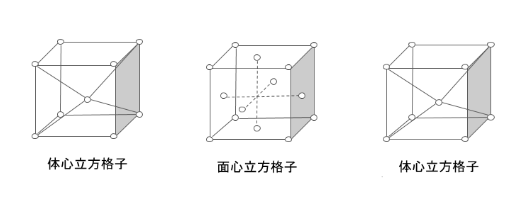
面心立方格子をもつ金属
面心立方格子の金属は展延性に富む特徴があるが、強さは劣る傾向にある。鉄(γ)、アルミニウム、ニッケル、金、銀、銅、鉛、白金などがある。
体心立方格子をもつ金属
体心立方格子の金属は硬度が強く、融点が高温である。鉄(α)、クロム、タングステンなどがある。
稠密六方格子をもつ金属
稠密六方格子の金属は脆く、展延性に劣る傾向にある。亜鉛、コバルト、チタン、マグネシウム、モリブデンなどがある。
変態
変態とは、化学組成は同一のまま、温度変化に伴い、物理的性質や原子配列が異なる物質へ変化することである。鋼や合金を熱処理した場合に起こる同一元素の集合状態の異なる変化を一般に相変態という。鉄の場合、常温では、鉄(Fe)は体心立方格子であるが、高温になると、鉄(Fe)は高温になると一定の温度で瞬間的に面心立方格子に変化する。
結晶粒
金属は、結晶格子を形作る単位胞が無数に集合して結晶体となる。さらに結晶体が集まって多結晶体を作り、それぞれが結晶粒を形成する。なお、結晶粒の境界は結晶粒界を作る。普通、多結晶体は降伏応力と結晶粒径の関係は、結晶粒が小さいほど強化する。このことをホールペッチの法則という。このことを利用して、金属の組成をそのままで結晶粒微細化を施すと、機械的性質が変わらずに結晶粒界の割合が増え、転位は結晶粒界を通り抜けるにくくなるため、大きなメリットがある。
塑性変形
金属は塑性変形すると、結晶粒を構成している原子が正規の配列から移動して乱れる。結晶粒にひずみが生じ、小さい外力がかかった場合は、原子の配列は外力が解放したときに元に戻り弾性変形のみで終わるが、大きい外力の場合は塑性変形を起こす。塑性変形を繰り返すと、変形が増すに従い硬度が増すが、このことを加工硬化や加工ひずみという。
加工硬化(加工ひずみ)
加工硬化(加工ひずみ)とは、材料に塑性変形を与えると、変形を繰り返すたびに変形に対する抵抗が増大して、変形を受けていない材料よりも硬くなる現象をいう。その原理については、塑性変形を繰り返すに伴い転位が増殖し、それが不均一な分布となり互いに絡み合う。そうすると、さらに外部から変形を起こそうとする力に対し、不均一な分布がそれを阻害しようとするため変形への抵抗が増す。加工硬化を生じた金属はもとの材料よりも降伏応力が増加し、硬度が増す一方、脆くなるというデメリットを持つ。脆さが問題となるときは焼きなましを施すことによって対処することが多い。圧延、鍛造、プレス成形、曲げ加工、ショットピーニングなどはこの加工硬化を利用した加工方法である。
析出
析出とは、固体中に拡散変態が進むと別の構造を持つ固体ができる現象である。アルミニウム合金やジュラルミンに代表される現象で、析出が起ると金属組織内にひずみ場ができるため、材料の硬度が大きくなる。溶媒原子が常温より多く固溶する高温まで加熱し、それを急冷させることで過飽和固溶体ができる。この過飽和固溶体は不安定な状態であるため、より安定な状態への過程として析出がある。
。