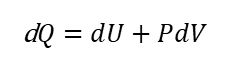熱力学第一法則
熱力学第一法則とは、熱は本質的には仕事と同じエネルギーの一形態であるといえ、仕事は熱に変えることもでき、また、熱を仕事に変えることもでき、熱と仕事の総和は変わらないという法則である。(参考:熱力学ゼロの法則、熱力学第二法則)
エネルギー保存の法則
エネルギー保存の法則(「ある状態で物体が保有するエネルギーの総和は、外部との間にエネルギーの交換がない限り一定不変である。」)から、熱力学第一法則においてもまた、エネルギーの総和は変わらない。
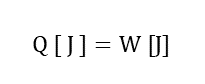
ジュールの実験
ジュールは、水の中に設置した羽根車とおもりをつなげた装置の実験で熱と仕事の関係を示した。ジュールの実験によると、おもりの重力運動で羽根車を回して水を攪拌し、停止した後の温度上昇を計測した。一方で、同じ温度変化は熱を加えることによっても可能であるため、熱と仕事は等しいものであるといえる。
シリンダとピストンの実験
シリンダとピストンで囲まれた状態にある気体に外部から熱量ΔQを加えて膨張したケースを考える。このモデルで与えた熱は、「気体が暖められるために使われたエネルギー」と「その体積を増加させるエネルギー」の総和に等しい、ということを示す。
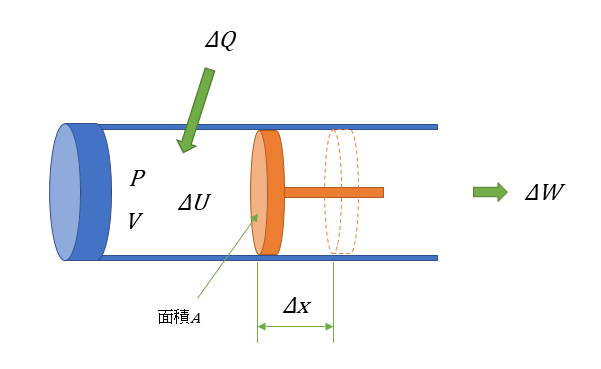
シリンダとピストン
熱量(ΔQ)は内部で増加したエネルギー(ΔU)と外部に仕事をしたエネルギー(ΔW)との総和に等しいので、次のような式になる。
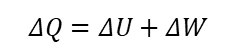
仕事量(ΔW)は、熱が加えられて容器の体積がΔVだけ増加して、ピストンが Δxの距離を移動したと考える。圧力Pが一定のとき、次のような式になる。
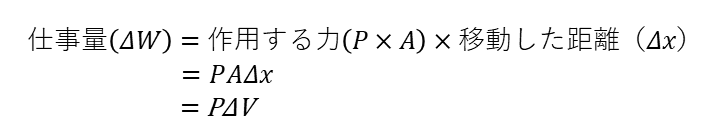
この式をΔQ=ΔU+ΔWの式に代入すると、

熱力学第一法則を期待について適用して微分形で示す。